Vertiefung

Hintergrund
[br]Die Versorgung dermatologischer Krankheiten beruht zu einem Großteil auf Arzneimitteltherapien. Mit topischen oder systemischen Therapeutika werden über 2.000 Krankheitsentitäten an der Haut versorgt. Nur für einen kleinen Teil dieser Krankheiten – in erster Linie für die häufigeren Dermatosen – liegen zu den eingesetzten Therapeutika Zulassungsstudien vor und können somit Verordnungen gemäß dem Zulassungsstatus erfolgen. Ein Großteil der dermatologischen Erkrankungen muss dementsprechend mit Arzneimitteln im Off-Label-Use (OLU) behandelt werden. Problemverstärkend wirkt sich aus, dass die Zulassungsstudien in den letzten Jahren immer stärker fokussierte Indikationen beinhalten und somit der Anteil an zulassungskonformen Behandlungssituationen weiter rückläufig ist. Sind beispielsweise in weit zurückliegenden Zulassungen wie bei den systemischen Glukokortikosteroiden noch Termini wie „bei entzündlichen Hautkrankheiten“ verwendet worden, so werden etwa die aktuell zugelassenen Calcineurininhibitoren eingeschränkt auf „nur bei schweren therapierefraktären Formen und fehlenden Behandlungsalternativen“. Ein weiterer gravierender Sachverhalt ist für die Verordnung von Dermatika bei seltenen Erkrankungen das geringere Aufkommen an Studiendaten trotz hoher Behandlungsnotwendigkeit. Trotz seiner hohen versorgerischen Bedeutung ist der Off-label-Use in der Dermatologie nur in wenigen wissenschaftlichen Arbeiten aufgegriffen worden und ist das Aufkommen an Publikationen hierzu gering. 1 2 3 In einer AOK-Studie aus Baden-Württemberg fanden sich bei Kindern von 0-16 Jahren im Jahr 1999 unter 1,7 Millionen Verordnungen insgesamt 13,2% im Off-label-Modus. 4 Die höchsten Raten wurden bei Augen-, HNO- und Hauterkrankungen gefunden (jeweils >60% OLU-Anteil), wobei lediglich Verordnungen von Allgemeinmedizinern, Kinderärzten und Internisten in die Analyse gelangten. Unter topischen Präparaten lag die Rate an OLU-Verordnungen bei 63,8%. In einer US-amerikanischen Analyse der landesweiten Verschreibungen in den Jahren 1990-1997 bei Hauterkrankungen wurden 200 Mio. Visiten ausgewertet. 5 32% aller Verordnungen waren „off-label“. Off-label Medikamente gehören damit nach dem Fazit der Autoren zum Standard der dermatologischen Behandlung. Eine französische Studie aus dem Jahre 2003 unterstreicht die Bedeutung des OLU in der Dermatologie. Hier wurden die Verordnungen der Clinique Dermatologique, Centre Hospitalier Universitaire Rouen analysiert. Der Anteil an OLU lag insgesamt bei 14% der dermatologischen Patienten. 6 Erst in den letzten Jahren wurden in mehreren Ländern Arbeitsgruppen tätig, die für einzelne Indikationen und Medikamente den Off-label use systematisch erarbeiteten, etwa bei Azathioprin 7, Ciclosporin A 8, Imiquimod 9, Acitretin 10, Allopurinol 11, Mycophenolatmofetil 12, Tacrolimus 13 14 oder Immunglobuline 15. Besonders intensiv wurden die monoklonalen Antikörper/Biologika auf ihre Eignung für weitere, außerhalb der Zulassungstexte liegenden Indikationen geprüft und diskutiert. 16 17 18 19 20 21 22[br][br]
Barrieren der Versorgung im Off-Label-Modus
[br]Auch bei eindeutiger medizinischer Indikation berichten viele Dermatologen in Praxis und Klinik über erhebliche Probleme im Off-Label-Bereich, insbesondere von höherpreisigen Arzneimitteln. Sowohl die medizinische Notwendigkeit (z. B. Diskussion der Krankheitsschwere) wie auch die Evidenz (Aussicht auf Therapieerfolg) werden nicht zuletzt von den MDKs und Krankenkassen nicht selten in Frage gestellt. Der unverhältnismäßig hohe bürokratische Aufwand und die nicht selten über viele Wochen verschleppte Behandlungszeit gehen zu Lasten der Versorgenden und ihrer Patienten. In einer Umfrage äußerten praktisch alle Dermatologen die Notwendigkeit des OLU und gaben über 90% Probleme mit der bürokratischen Abwicklung an.[br][br]
Dermatologisch relevante Arzneimittel mit bedeutenden Off-Label-Indikationen
[br]In der Dermatotherapie wird eine große Zahl von Arzneimitteln ohne entsprechenden Zulassungsstatus benötigt. Hierzu zählen insbesondere Immunsuppressiva und immunmodulierende Substanzen, aber auch Therapeutika für andere Indikationen (Tab. 1).[br][br]
Wichtige Indikationen mit Bedarf nach Off-Label-Use
[br]Unter der großen Zahl von Erkrankungen, für die Arzneimittel mit Zulassungsstatus fehlen, hat eine Arbeitsgruppe der DDG wichtige Zielindikationen definiert, die zukünftig in Form einer Positiv-Liste einmalig und verbindlich geklärt werden sollten (Tab. 1). Hierzu zählen insbesondere Autoimmunerkrankungen der Haut, seltenere entzündliche Erkrankungen sowie Wundkrankheiten und dermato-onkologische Indikationen (Tab. 2). Mit Blick auf häufige dermatologische Indikationen ohne ausreichende Arzneimittelzulassungen sind seltenere Erkrankungen und komplexe Leiden ohne dermatologische Kernindikationen besonders häufig betroffen. Für die Behandlung der systemischen Sklerodermie liegen beispielsweise mit den Glukokortikoidsteroiden und Cyclophosphamid nur zwei Medikamente vor, die zulassungskonform eingesetzt werden können. Ein weitaus größerer Anteil an benötigten Medikamenten muss stattdessen ohne Zulassungsstatus eingesetzt werden.[br][br]
Systematik der sachgerechten Arzneimittelverordnung im Off-Label-Use
[br]
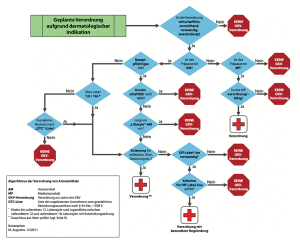
Abb. 1: Schematisches Vorgehen bei der sachgerechten Verordnung von Arzneimitteln und Medizinprodukten (nach: Augustin M et al., www.arzneimittelleitfaden.de)
Innerhalb des Entscheidungsganges zu einer sachgerechten Verordnung in der vertragsärztlichen Versorgung stellt sich die Frage nach dem OLU grundsätzlich, wenn der vorgesehene Wirkstoff ein Arzneimittel darstellt und keiner weiteren Einschränkung durch das Wirtschaftlichkeitsgebot und die Arzneimittelrichtlinien unterliegt (Abb. 1). Im Regelfalle ist bei fehlender zulassungskonformer Anwendung keine Verordnung zu Lasten der GKV möglich. Wenn ein für die medizinische Indikation zweckmäßiges, ausreichendes und wirtschaftliches Arzneimittel verordnet werden soll, die Zulassung hierfür jedoch nicht gegeben ist (Abb. 1), dann ist die Frage der Notwendigkeit nochmals kritisch u prüfen. Liegt auch diese vor, so gilt es die Kriterien des OLU zu prüfen. Sind diese erfüllt, sollte eine Verordnung mit besonderer Begründung angestrebt werden. Im anderen Falle ist die Verordnung zu Lasten der GKV nicht möglich.Stattdessen sollte mit dem Patienten gemeinsam geklärt werden, ob ein Selbstkauf des Arzneimittels möglich ist.[br][br]
Hinweise für die Verordnung von Dermatika im Off-Label-Modus
[br]Die Verordnung von Medikamenten im Off-Label-Modus kann bei sachgerechter Anwendung der gesetzlichen Bestimmungen und bei Beachtung der formellen Anforderungen fast immer ohne Regressrisiko durchgeführt werden. Allerdings ist damit ein erhöhter Aufwand verbunden, der für die Routineversorgung häufig inakzeptabel erscheint. Sieht der behandelnde Arzt die Voraussetzungen eines Off-Label-Use als gegeben an, sollte er bei der Krankenkasse als Kostenträger deren schriftliche Zustimmung zur Erstattungsfähigkeit einholen. Erfolgt die Zustimmung des Kostenträgers, kann ein Kassenrezept ausgestellt werden. Stellt der Arzt ohne vorherige Zusage des Kostenträgers ein Kassenrezept aus, dann besteht das Risiko, dass er in Regress genommen wird und die Frage, ob ein Off-Label-Use vorgelegen hat, wird im Regressverfahren abzuklären sein. Lehnt die Krankenkasse die Erstattungsfähigkeit ab oder holt der Arzt bei dem Kostenträger keine vorherige Auskunft ein, dann sollte er dem Patienten ein Privatrezept ausstellen und es ihm überlassen, sich bei der Krankenkasse um Erstattung zu bemühen. Eine effektivere Arzneimitteltherapie kann dementsprechend vor allem durch eine stärkere Standardisierung sowie durch Nutzung vorhandener Ressourcen wie der Datenbank des SOLUderm erreicht werden. Diese Datenbank baut Wissen und Erfahrungen in der Durchführung des OLU bei Hautkrankheiten auf. Sie bietet für viele Indikationen die notwendige Datengrundlage an und fasst für die Begründung der Off-Label-Verordnungen das Aufkommen an Evidenz (Aussichten auf Behandlungserfolg) zusammen. Für Dermatologen ist die Nutzung dieser Datenbank kostenfrei.[br][br]
Zukünftige Handlungsbedarfe
[br]Der Off-Label-Status zahlreicher dermatotherapeutischer Medikamente ist nicht durch medizinische, sondern formelle Determinanten begründet. Diese dürfen dem Anspruch des Patienten auf die notwendige und zweckmäßige Therapie sowie insbesondere dem Gebot der ethisch motivierten, humanen Krankenbehandlung nicht im Wege stehen. Die vermeintliche Abwendung von Schäden durch die Arzneimitteltherapie ist nur in den seltensten Fällen ein hinreichender Grund zur Unterlassung einer entsprechenden Off-Label-Therapie. Bei den meisten auch vorgenannten Therapeutika sind vielmehr das Nebenwirkungsspektrum und das Schadenspotential bereits bekannt und kann eine sorgfältige Nutzen-Risiko-Abwägung ohne weiteres getroffen werden. Vor diesem Hintergrund ist es dringend notwendig, eine klare, den Patienteninteressen entsprechende und zugleich den Arzt schützende, einheitliche Sachlage für den OLU herbeizuführen. Angesichts der weiterhin bestehenden Restriktionen sollte dies idealerweise eine Positiv-Liste mit rational begründeten Therapiehinweisen für den geschützten OLU sein. Solange eine entsprechende klare Listung von Indikationen nicht vorliegt, bedarf es eines erheblichen Mehraufwandes für die verordnenden Dermatologen, um in allen medizinisch begründeten und vertretbaren Fällen den Patienten die ihnen zustehende Arzneimittelversorgung zukommen zu lassen. Die Kenntnis der dafür wichtigen Bestimmungen sowie die gute Dokumentation sind essentiell.[br][br]
Unterstützung der Arzneimittelversorgung im Off-Label-Use durch das Projekt „SOLUderm“
[br]In diesem Projekt unterstützen das CVderm und das Iderm in Kooperation mit dem Berufsverband der Deutschen Dermatologen (federführend Prof. Dr. Fritz) die verordnenden Dermatologen mit einer Datenbank von gesicherten Anwendungen und einschlägiger unterstützender Literatur zum OLU.
Literatur
| ↑1 | Li VW, Jaffe MP, Li WW, Haynes HA. Off-label dermatologic therapies. Usage, risks, and mechanisms. Arch Dermatol. 1998 Nov;134(11):1449-54. (Link zur Artikelseite | PDF anfordern) |
|---|---|
| ↑2 | Brunne V, Mertins G, Reimann G, Brockmeyer NH. Off-label use in der Dermatologie. Hautarzt 2004; 55:727–734. (Link zur Artikelseite | PDF anfordern) |
| ↑3 | Brockmeyer NH, Brucklacher U, Potthoff A, Reich-Schupke S. Off-label use in der Dermatologie in Deutschland: Was hat sich seit 2004 verändert? J Dtsch Dermatol Ges. 2009 Nov;7(11):938-45. (Link zur Artikelseite | PDF anfordern) |
| ↑4 | Bücheler R, Schwab M, Mörike K, Kalchthaler B, Mohr H, Schröder H, Schwoerer P, Gleiter CH. Off label prescribing to children in primary care in Germany: retrospective cohort study. BMJ. 2002 Jun 1;324(7349):1311-2. (Link zur Artikelseite | PDF anfordern) |
| ↑5 | Sugarman JH, Fleischer AB Jr, Feldman SR. Off-label prescribing in the treatment of dermatologic diseases. J Am Acad Dermatol. 2002 Aug;47(2):217-23. (Link zur Artikelseite | PDF anfordern) |
| ↑6 | Picard D, Carvalho P, Bonnavia C, Louin L, Josset V, Lauret P, Joly P. Assessment off-label prescribing in Dermatology. [Article in French]. Ann Dermatol Venereol. 2003 May;130(5):507-10. (Link zur Artikelseite | PDF anfordern) |
| ↑7 | Schram ME, Borgonjen RJ, Bik CM, van der Schroeff JG, van Everdingen JJ, Spuls PI; Off-Label Working and Project Group of Dutch Society of Dermatology and Venereology. Off-label use of azathioprine in dermatology: a systematic review. Arch Dermatol. 2011 Apr;147(4):474-88. (Link zur Artikelseite | PDF anfordern) |
| ↑8 | Dehesa L, Abuchar A, Nuno-Gonzalez A, Vitiello M, Kerdel FA.The use of cyclosporine in dermatology. J Drugs Dermatol. 2012 Aug;11(8):979-87. ( |
| ↑9 | David CV, Nguyen H, Goldenberg G. Imiquimod: a review of off-label clinical applications. J Drugs Dermatol. 2011 Nov;10(11):1300-6. ( |
| ↑10 | Dunn LK, Gaar LR, Yentzer BA, O’Neill JL, Feldman SR. Acitretin in dermatology: a review. J Drugs Dermatol. 2011 Jul;10(7):772-82. ( |
| ↑11 | Tsai TF, Yeh TY. Allopurinol in dermatology. Am J Clin Dermatol. 2010;11(4):225-32. (Link zur Artikelseite | PDF anfordern) |
| ↑12 | Orvis AK, Wesson SK, Breza TS Jr, Church AA, Mitchell CL, Watkins SW. Mycophenolate mofetil in dermatology. J Am Acad Dermatol. 2009 Feb;60(2):183-99. (Link zur Artikelseite | PDF anfordern) |
| ↑13 | Sehgal VN, Srivastava G, Dogra S. Tacrolimus: approved and unapproved dermatologic indications/uses-physician’s sequential literature survey: part II. Skinmed. 2008 Mar-Apr;7(2):73-7. ( |
| ↑14 | UR Hengge, A Marini. Spezielle Behandlungsoptionen mit topischem Tacrolimus. Georg Thieme Verlag, Stuttgart, New York, 2007. ( |
| ↑15 | Fernandez AP, Kerdel FA. The use of i.v. IG therapy in dermatology. Dermatol Ther. 2007 Jul- Aug;20(4):288-305. Review. (Link zur Artikelseite | PDF anfordern) |
| ↑16 | Sockolov ME, Alikhan A, Zargari O. Non-psoriatic dermatologic uses of monoclonal antibody therapy. J Dermatolog Treat. 2009;20(6):319-27. (Link zur Artikelseite | PDF anfordern) |
| ↑17 | Díaz-Ley B, Guhl G, Fernández-Herrera J. Off-label use of biologic agents in the treatment of dermatosis, Part 1: infliximab and adalimumab. Actas Dermosifiliogr. 2007 Dec;98(10):657-78. Review. (Link zur Artikelseite | PDF anfordern) |
| ↑18 | Guhl G, Díaz-Ley B, Fernández-Herrera J. Off-label use of biologic agents in the treatment of dermatosis, part 2: etanercept, efalizumab, alefacept, rituximab, daclizumab, basiliximab, omalizumab, and cetuximab]. Actas Dermosifiliogr. 2008 Jan-Feb;99(1):5-33. (Link zur Artikelseite | PDF anfordern) |
| ↑19 | Carr DR, Heffernan MP. Off-label uses of rituximab in dermatology. Dermatol Ther. 2007 Jul- Aug;20(4):277-87. (Link zur Artikelseite | PDF anfordern) |
| ↑20 | Smith DI, Swamy PM, Heffernan MP. Off-label uses of biologics in dermatology: interferon and intravenous immunoglobulin (part 1 of 2). J Am Acad Dermatol. 2007 Jan;56(1):e1-54. Epub 2006 Nov 7. (Link zur Artikelseite | PDF anfordern) |
| ↑21 | Graves JE, Nunley K, Heffernan MP. Off-label uses of biologics in dermatology: rituximab, omalizumab, infliximab, etanercept, adalimumab, efalizumab, and alefacept (part 2 of 2). J Am Acad Dermatol. 2007 Jan;56(1):e55-79. Epub 2006 Nov 7. (Link zur Artikelseite | PDF anfordern) |
| ↑22 | Kerns MJ, Graves JE, Smith DI, Heffernan MP. Off-label uses of biologic agents in dermatology: a 2006 update. Semin Cutan Med Surg. 2006 Dec;25(4):226-40. Review. ( |
